La farmacogenetica e la psichiatria moderna affronta una grande sfida clinica: la variabilità della risposta dei pazienti ai trattamenti farmacologici.
È esperienza comune per gli psichiatri osservare pazienti che, pur condividendo la stessa diagnosi e ricevendo lo stesso farmaco e la stessa dose, reagiscono in modi radicalmente diversi.
Alcuni mostrano una rapida remissione dei sintomi, altri ottengono miglioramenti parziali o limitati, mentre altri ancora manifestano importanti effetti collaterali o addirittura nessuna risposta terapeutica.
La possibilità di prevedere con precisione la risposta di un paziente a un determinato trattamento è attualmente limitata. Di conseguenza, la pratica clinica tradizionale è caratterizzata da un approccio basato prevalentemente sul “tentativo ed errore”.
Questo metodo, seppur necessario, può comportare un considerevole ritardo nel raggiungimento dell’efficacia terapeutica, un maggiore rischio di effetti collaterali e, non da ultimo, un significativo impatto negativo sulla qualità di vita dei pazienti.
Di fronte a queste criticità sta emergendo sempre più chiaramente la necessità di adottare strategie terapeutiche che siano mirate e personalizzate, capaci cioè di integrare le caratteristiche biologiche e genetiche specifiche di ciascun individuo.
Punti chiave
- Basta “Prova ed Errore”: La psichiatria lotta con risposte variabili ai farmaci; la farmacogenetica offre una via d’uscita dall’approccio “tenta e riprova”.
- Personalizzazione Cruciale: La farmacogenetica emerge come strumento chiave per terapie psichiatriche “su misura”, basate sul profilo biologico e genetico del paziente.
- Genetica in Farmacia: È la scienza che studia come le variazioni genetiche individuali influenzano la risposta ai farmaci, mirando alla scelta del medicinale e della dose più efficaci.
- CYP450: Il Metabolizzatore: Gli enzimi CYP (specialmente il CYP2D6) sono cruciali per il metabolismo di molti psicofarmaci; variazioni genetiche in questi enzimi alterano efficacia e sicurezza.
- CYP2D6: Il Genio della Psichiatria: Questo enzima metabolizza moltissimi antidepressivi e antipsicotici. Testare il CYP2D6 aiuta a prevedere la risposta e a evitare dosi inefficaci o tossiche.
- Genotipo vs. Fenotipo: Non solo il “codice” genetico (genotipo), ma anche come si manifesta (fenotipo metabolico, es. metabolizzatore lento o rapido) è fondamentale per aggiustare le dosi.
- Il Futuro è Integrato: La psichiatria di domani combinerà farmacogenetica, biomarcatori e monitoraggio clinico per trattamenti personalizzati e basati sull’evidenza.

- Punti chiave
- La variabilità individuale nella risposta farmacologica
- Cos’è la farmacogenetica e perchè è così importante
- Farmacogenetica: la scienza dietro la variabilità terapeutica
- Dal laboratorio alla clinica: l’importanza del test CYP2D6
- La promessa della farmacogenetica integrata: come cambierà la psichiatria?
- Potenzialità e vantaggi del modello integrato
- Conclusioni
La variabilità individuale nella risposta farmacologica
La variabilità individuale nella risposta ai farmaci è il risultato di un’interazione complessa tra molteplici fattori. Alcuni di questi sono ben noti e facilmente identificabili, come età, sesso, peso corporeo e comorbidità mediche; altri, invece, sono di natura genetica e quindi meno evidenti, sebbene abbiano un’importanza clinica spesso decisiva.
Fra i fattori genetici che influenzano questa variabilità ci sono le differenze individuali nel metabolismo dei farmaci, dovute alla presenza di varianti genetiche (polimorfismi) nei geni che codificano gli enzimi metabolizzatori.
- Ad esempio, gli enzimi della famiglia del citocromo P450 (CYP), in particolare l’enzima CYP2D6, presentano numerose varianti che determinano la capacità individuale di metabolizzare molti farmaci psichiatrici come antidepressivi, antipsicotici e stabilizzatori dell’umore.
Queste differenze genetiche possono portare a significative variazioni nella concentrazione plasmatica e tissutale dei farmaci, determinando così sia la loro efficacia clinica sia la loro sicurezza.
La capacità di identificare preventivamente tali differenze rappresenta un obiettivo primario della ricerca farmacologica contemporanea e una promettente prospettiva per la clinica psichiatrica futura.
Cos’è la farmacogenetica e perchè è così importante
La farmacogenetica è la branca della genetica applicata alla farmacologia che studia come le varianti genetiche individuali possano influenzare la risposta ai farmaci.
L’obiettivo principale della farmacogenetica è quindi la personalizzazione della terapia farmacologica, ovvero la possibilità di scegliere il farmaco più adatto e la dose ottimale per ciascun paziente sulla base delle sue caratteristiche genetiche.
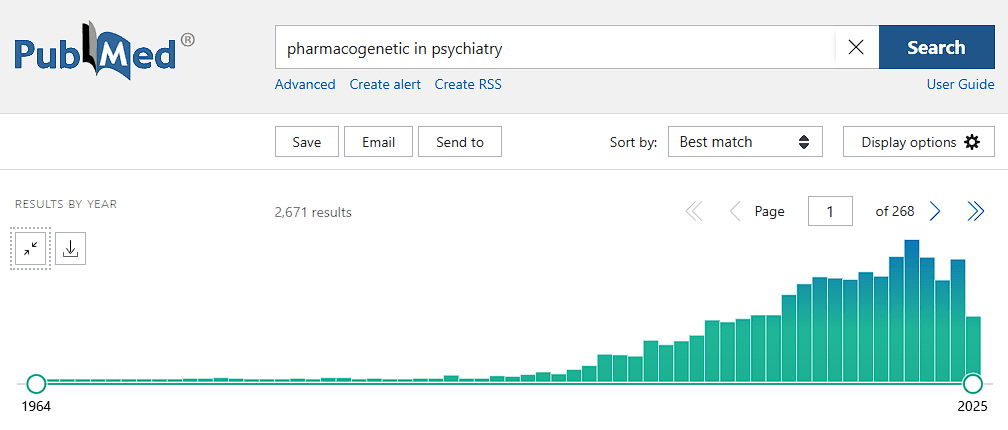
Negli ultimi decenni come visibile nell’istogramma delle pubblicazioni presenti e catalogate su PubMed, la farmacogenetica ha acquisito crescente rilevanza in ambito psichiatrico, soprattutto a causa delle difficoltà riscontrate nel trattamento di condizioni come la depressione maggiore, la schizofrenia e il disturbo bipolare, patologie per le quali la risposta farmacologica è spesso imprevedibile.
Pur essendo ancora in fase di sviluppo e perfezionamento, la farmacogenetica ha già mostrato risultati incoraggianti nella gestione terapeutica individualizzata, contribuendo a ridurre la frequenza e la gravità degli effetti collaterali e aumentando l’efficacia complessiva del trattamento.
L’applicazione clinica della farmacogenetica rappresenta un passo avanti fondamentale per superare il tradizionale approccio empirico e consentire finalmente un trattamento psichiatrico davvero su misura, basato su solide evidenze scientifiche.
Farmacogenetica: la scienza dietro la variabilità terapeutica
La farmacogenetica è quindi la disciplina scientifica che esplora la relazione tra le caratteristiche genetiche individuali e la risposta ai farmaci. In altre parole, essa studia come varianti specifiche presenti nel DNA di una persona influenzino il metabolismo, l’efficacia e la tollerabilità di un determinato trattamento farmacologico.
Al centro della farmacogenetica troviamo il concetto di polimorfismo genetico, ovvero piccole differenze nella sequenza del DNA tra individui della stessa specie. Questi polimorfismi spesso coinvolgono geni responsabili della sintesi di enzimi chiave nella metabolizzazione dei farmaci, come quelli appartenenti alla famiglia del citocromo P450.
Il risultato di tali differenze genetiche può tradursi in diverse capacità metaboliche, influenzando pertanto la dose necessaria per raggiungere una determinata efficacia terapeutica, la durata dell’azione farmacologica e l’incidenza di eventuali effetti collaterali.
In sostanza, il principio chiave della farmacogenetica è la possibilità di utilizzare informazioni genetiche per ottimizzare la terapia farmacologica, riducendo gli errori terapeutici e incrementando la sicurezza e l’efficacia complessiva dei trattamenti.
Differenza tra farmacogenetica e farmacogenomica
Nonostante i termini “farmacogenetica” e “farmacogenomica” siano spesso utilizzati come sinonimi, essi indicano concetti leggermente diversi.
- La farmacogenetica, termine introdotto per la prima volta negli anni ‘50, si riferisce come abbiamo detto principalmente allo studio delle singole varianti genetiche (solitamente singoli polimorfismi nucleotidici, detti SNP) e al loro effetto diretto sul metabolismo dei farmaci e sulla risposta clinica.
- La farmacogenomica, invece, è un concetto più recente che amplia notevolmente questo approccio. Essa prende in considerazione l’intero genoma del paziente, analizzando non solo singoli geni, ma anche gruppi di geni e reti complesse di interazioni genetiche che possono influenzare globalmente la risposta ai farmaci. La farmacogenomica integra strumenti tecnologici avanzati, come l’analisi di espressione genica e tecniche di sequenziamento genetico ad alto rendimento per ottenere una visione più completa e dettagliata della risposta terapeutica individuale.
Mentre la farmacogenetica ha un approccio mirato, focalizzato su pochi geni specifici e chiaramente identificati, la farmacogenomica mira a offrire una visione globale e integrata della genetica umana applicata alla medicina personalizzata.
Il ruolo degli enzimi di metabolizzazione
Gli enzimi appartenenti alla famiglia del citocromo P450 svolgono un ruolo fondamentale nella metabolizzazione della maggior parte dei farmaci prescritti in medicina e in psichiatria. Questi enzimi sono principalmente localizzati nel fegato e agiscono favorendo la conversione delle molecole farmacologiche in metaboliti, solitamente più idrosolubili, facilitando così la loro eliminazione dall’organismo.
La famiglia del citocromo P450 comprende numerosi isoenzimi (varianti), ciascuno caratterizzato da una specifica attività catalitica e da un proprio spettro di substrati farmacologici (ovvero di target). I più rilevanti nella metabolizzazione dei farmaci psichiatrici includono CYP1A2, CYP2C9, CYP2C19, CYP2D6 e CYP3A4. Ognuno di questi isoenzimi può mostrare una notevole variabilità genetica tra gli individui, determinando significative differenze nella velocità e nell’efficienza con cui i farmaci vengono metabolizzati.
La comprensione di come questi enzimi influenzino la concentrazione plasmatica e tissutale dei farmaci rappresenta un passaggio cruciale per ottimizzare il trattamento psichiatrico, minimizzare gli effetti collaterali e massimizzare l’efficacia terapeutica.

L’isoenzima CYP2D6 in psichiatria
Tra tutti gli isoenzimi citocromo P450, il CYP2D6 occupa una posizione di particolare rilievo in ambito psichiatrico. Questo enzima è coinvolto nel metabolismo di una vasta gamma di psicofarmaci comunemente utilizzati, inclusi:
- antidepressivi triciclici (ad es. amitriptilina, nortriptilina, imipramina), SSRI (paroxetina, fluoxetina),
- inibitori selettivi della ricaptazione di serotonina e noradrenalina (venlafaxina, duloxetina),
- antipsicotici come risperidone e aripiprazolo.
Come detto l’attività metabolica del CYP2D6 può variare considerevolmente tra individui a causa della presenza di diverse varianti genetiche, o polimorfismi.
Alcuni di questi polimorfismi determinano una significativa riduzione o addirittura la completa inattivazione dell’attività enzimatica, mentre altri possono condurre a una iperattività metabolica.
Proprio per la sua ampia partecipazione nella metabolizzazione degli psicofarmaci, la caratterizzazione genetica dell’enzima CYP2D6 è uno degli strumenti farmacogenetici più utilizzati e clinicamente validati in psichiatria. Il test genetico per CYP2D6 può infatti aiutare a predire la risposta terapeutica, evitando dosaggi inefficaci o tossici, e suggerendo eventuali cambiamenti di farmaco prima ancora che insorgano problemi clinici rilevanti.
Genotipo vs Fenotipo: come influenzano la terapia
Per comprendere appieno la farmacogenetica e il suo impatto clinico, è essenziale chiarire la differenza tra due concetti fondamentali: genotipo e fenotipo.
- Il genotipo rappresenta l’insieme specifico di informazioni genetiche di un individuo, ovvero la sequenza esatta di DNA presente nei suoi geni. Nel contesto della farmacogenetica, il genotipo indica la presenza di particolari varianti genetiche (polimorfismi), che determinano la struttura e la funzione degli enzimi coinvolti nel metabolismo dei farmaci.
- Il fenotipo, invece, è la manifestazione osservabile e misurabile del genotipo. In farmacogenetica, il fenotipo corrisponde, ad esempio, alla capacità effettiva di un paziente di metabolizzare un farmaco. Questa capacità, influenzata dal genotipo, determina la velocità con cui il farmaco viene eliminato dal corpo e la sua concentrazione plasmatica finale.
È importante sottolineare che il fenotipo, pur essendo fortemente influenzato dal genotipo, può essere modificato anche da fattori non genetici, come età, interazioni farmacologiche, malattie concomitanti, dieta e condizioni ambientali.

Fenotipi metabolici: metabolizzatori lenti, intermedi, rapidi e ultrarapidi
La variabilità genetica nell’enzima CYP2D6 determina quattro principali categorie fenotipiche (o caratteristiche rilevabili nella clinica) ognuna associata a una differente velocità metabolica:
- Metabolizzatori lenti (poor metabolizers – PM): individui con completa inattivazione o assenza di attività enzimatica. Questi pazienti rischiano accumuli tossici del farmaco a dosi standard, presentando spesso effetti collaterali significativi anche a bassi dosaggi. Pazienti con scarsa o assente attività enzimatica richiedono spesso una significativa riduzione della dose standard. Ad esempio, con antidepressivi triciclici come la nortriptilina o la desipramina, è spesso necessario dimezzare o addirittura ridurre a un quarto la dose iniziale raccomandata per prevenire tossicità e gravi effetti collaterali.
- Metabolizzatori intermedi (intermediate metabolizers – IM): presentano un’attività enzimatica parzialmente ridotta rispetto alla media della popolazione. Possono necessitare di un aggiustamento moderato della dose per evitare effetti avversi e mantenere l’efficacia terapeutica. Questi pazienti presentano una moderata riduzione della capacità metabolica; solitamente richiedono aggiustamenti intermedi della dose (circa 20-50% inferiore rispetto alla dose standard). Nel caso della paroxetina, ad esempio, è consigliabile iniziare con dosaggi lievemente inferiori rispetto a quelli comunemente utilizzati.
- Metabolizzatori rapidi o normali (extensive metabolizers – EM): rappresentano la categoria più comune nella popolazione generale, caratterizzati da una normale attività enzimatica. Generalmente rispondono bene alle dosi standard raccomandate dai protocolli clinici. Generalmente questi pazienti non necessitano di alcun adattamento particolare rispetto alle dosi raccomandate nelle linee guida terapeutiche standard. In questo caso, il test genetico conferma la possibilità di proseguire con una terapia convenzionale.
- Metabolizzatori ultrarapidi (ultrarapid metabolizers – UM): individui che possiedono copie multiple funzionali del gene CYP2D6, con conseguente attività enzimatica molto elevata. Tali pazienti possono richiedere dosaggi superiori rispetto a quelli standard, poiché il farmaco viene rapidamente metabolizzato, riducendone efficacia e durata d’azione. Nei pazienti con capacità metaboliche particolarmente elevate, è necessario incrementare la dose iniziale, talvolta fino al doppio della dose raccomandata, oppure scegliere farmaci non significativamente metabolizzati da CYP2D6 per ottenere un effetto terapeutico adeguato. Ad esempio, un paziente ultrarapido che assume amitriptilina potrebbe richiedere dosaggi superiori rispetto agli standard clinici usuali o un cambiamento di molecola.
Esempi pratici con antidepressivi e antipsicotici
Ecco alcuni esempi clinici molto significativi che aiutano a comprendere come le differenze genetiche possano avere implicazioni concrete nella gestione terapeutica.
- Antidepressivi triciclici (es. amitriptilina, nortriptilina)
Questi farmaci vengono principalmente metabolizzati dal CYP2D6. Nei metabolizzatori lenti, dosaggi standard provocano facilmente livelli plasmatici elevati del farmaco, causando tossicità con effetti collaterali importanti, come sonnolenza, vertigini e problemi cardiaci. Nei metabolizzatori ultrarapidi, invece, dosi standard potrebbero risultare inefficaci, richiedendo aumenti di dosaggio per raggiungere una risposta terapeutica adeguata. - Inibitori selettivi della ricaptazione della serotonina (SSRI, es. paroxetina, fluoxetina)
La paroxetina, metabolizzata dal CYP2D6, può accumularsi nei metabolizzatori lenti, causando effetti collaterali come aumento dell’ansia, disfunzioni sessuali o disturbi gastrointestinali. Al contrario, in pazienti ultrarapidi, potrebbe verificarsi una mancata risposta terapeutica a causa di livelli plasmatici troppo bassi. - Antipsicotici atipici (es. risperidone, aripiprazolo)
Il risperidone viene trasformato dal CYP2D6 in un metabolita attivo, il paliperidone. Nei metabolizzatori lenti si osservano alte concentrazioni di risperidone rispetto al metabolita attivo, aumentando la probabilità di effetti collaterali extrapiramidali (tremori, rigidità, irrequietezza motoria). Nei metabolizzatori ultrarapidi, invece, si verifica una rapida conversione al metabolita, con una possibile variazione nella risposta clinica che richiede specifici aggiustamenti della terapia.
Tabella illustrativa con percentuali di adattamento per antidepressivi comuni
Di seguito una tabella sintetica e illustrativa dei principali adattamenti percentuali della dose raccomandati in base al fenotipo CYP2D6, per alcuni antidepressivi di uso frequente:
| Farmaco | Metabolizzatori Lenti (PM) | Metabolizzatori Intermedi (IM) | Metabolizzatori Rapidi (EM) | Metabolizzatori Ultrarapidi (UM) |
|---|---|---|---|---|
| Amitriptilina | -50/70% ↓ | -25/50% ↓ | Nessun adattamento | +50/100% ↑ |
| Nortriptilina | -50/70% ↓ | -25/50% ↓ | Nessun adattamento | +50/100% ↑ |
| Imipramina | -50% ↓ | -25/50% ↓ | Nessun adattamento | +50/100% ↑ |
| Paroxetina | -50% ↓ | -25% ↓ | Nessun adattamento | +50% ↑ |
| Venlafaxina | -30/50% ↓ | -25% ↓ | Nessun adattamento | +50% ↑ |
Legenda: ↓ riduzione della dose, ↑ incremento della dose.
Questi dati illustrativi forniscono un punto di riferimento generale, che deve sempre essere integrato da un attento giudizio clinico basato sulla risposta individuale e sul monitoraggio terapeutico dei farmaci (TDM).
L’approccio farmacogenetico alla prescrizione psichiatrica, pertanto, rimane complementare e sinergico rispetto all’esperienza clinica del professionista.

Dal laboratorio alla clinica: l’importanza del test CYP2D6
Nella pratica psichiatrica quotidiana l’imprevedibilità della risposta farmacologica rappresenta una delle sfide più complesse e impegnative. Il test genetico per l’enzima CYP2D6 offre una soluzione concreta, fondata su solide basi scientifiche, che permette di personalizzare la terapia farmacologica e ridurre il margine di errore terapeutico.
Razionale per il test CYP2D6: casi clinici
Per comprendere l’importanza del test CYP2D6, consideriamo alcuni esempi clinici rappresentativi:
- Caso 1: paziente con depressione resistente
Un paziente trattato con dosi standard di antidepressivi triciclici, nonostante l’aderenza terapeutica, non mostra alcuna risposta clinica apprezzabile dopo diverse settimane di terapia. Il test CYP2D6 rivela un fenotipo di metabolizzatore ultrarapido: in questo caso, un semplice aumento del dosaggio o il passaggio a farmaci metabolizzati diversamente potrebbe risolvere il problema, evitando lunghe e inutili sofferenze per il paziente. - Caso 2: tossicità da paroxetina
Una giovane donna trattata con paroxetina riferisce gravi effetti collaterali (agitazione, insonnia, tremori e disturbi gastrointestinali). Il test rivela un fenotipo di metabolizzatore lento CYP2D6. Riducendo la dose o sostituendo la paroxetina con un farmaco non metabolizzato dal CYP2D6, la paziente sperimenta una significativa riduzione degli effetti avversi. - Caso 3: effetti collaterali da risperidone
Un paziente con schizofrenia mostra effetti collaterali extrapiramidali (tremore, rigidità muscolare e acatisia) a dosaggi standard di risperidone. Il test CYP2D6 conferma un fenotipo di metabolizzatore lento. Sostituendo il farmaco o abbassando la dose in base al risultato del test, si ottiene un miglior controllo dei sintomi psicotici senza gli effetti collaterali precedentemente riportati.
Situazioni cliniche in cui il test è più efficace
L’utilità clinica del test genetico CYP2D6 varia in base a diversi fattori clinici e farmacologici. Esso risulta particolarmente indicato e efficace nelle seguenti situazioni:
- Trattamento di pazienti resistenti ai farmaci
In pazienti che non rispondono ai farmaci a dosaggi terapeutici standard, il test genetico può fornire informazioni cruciali per orientare rapidamente la scelta di dosaggi più appropriati o di farmaci alternativi. - Comparsa di effetti collaterali inattesi e severi
Quando i pazienti manifestano effetti collaterali gravi o insoliti rispetto alla popolazione generale, la determinazione del genotipo può identificare prontamente se la causa è attribuibile a un metabolismo alterato mediato dal CYP2D6. - Polifarmacoterapia complessa
Nei pazienti anziani, nei pazienti con comorbidità mediche, e in coloro che assumono contemporaneamente più farmaci, il test genetico aiuta a individuare preventivamente interazioni farmacocinetiche potenzialmente pericolose. - Terapie con farmaci a stretto indice terapeutico
Per i farmaci con una finestra terapeutica molto ristretta (come gli antidepressivi triciclici), il test CYP2D6 assume una particolare importanza clinica, permettendo di raggiungere rapidamente il giusto equilibrio tra efficacia e sicurezza.
Necessità di monitorare la concentrazione plasmatica o TDM
Nonostante la validità dei test genetici per CYP2D6, la concentrazione plasmatica del farmaco rimane un parametro essenziale da monitorare nella pratica clinica. Infatti, la farmacocinetica di molti farmaci psichiatrici è influenzata non solo dalla genetica, ma anche da numerosi altri fattori come età, peso corporeo, interazioni farmacologiche, patologie concomitanti, abitudini di vita e aderenza terapeutica.
La combinazione del test genetico con il monitoraggio terapeutico del farmaco (TDM, Therapeutic Drug Monitoring) offre quindi un approccio ancora più preciso e completo.
La misurazione diretta della concentrazione plasmatica consente infatti di verificare che il farmaco si trovi effettivamente nella finestra terapeutica desiderata, ottimizzando ulteriormente la sicurezza e l’efficacia del trattamento.
Limiti e sfide degli adattamenti della dose
Sebbene l’adattamento della dose basato sul genotipo rappresenti un grande progresso nella medicina personalizzata, esistono alcune limitazioni da considerare:
- Variabilità clinica individuale:
Anche con la conoscenza del genotipo, altri fattori come età, peso, malattie concomitanti e interazioni farmacologiche possono influenzare notevolmente la risposta terapeutica, rendendo necessario un monitoraggio clinico attento e continuativo. - Eterogeneità degli studi disponibili:
Molti adattamenti di dose derivano da studi condotti prevalentemente su volontari sani e non sempre rappresentativi delle reali popolazioni cliniche, il che potrebbe limitare la generalizzabilità dei risultati ottenuti. - Ruolo dei metaboliti farmacologicamente attivi:
Alcuni farmaci producono metaboliti attivi (come il risperidone che viene convertito in paliperidone). In questi casi, il semplice adattamento della dose basato sul genotipo del CYP2D6 potrebbe non essere sufficiente, poiché anche i metaboliti attivi vanno considerati nel determinare l’effetto clinico finale. - Costi e accessibilità dei test genetici:
Sebbene i costi dei test farmacogenetici stiano diminuendo, la loro diffusione è ancora limitata da questioni economiche, logistiche e dalla formazione specifica necessaria per interpretarne correttamente i risultati nella pratica clinica quotidiana.
La promessa della farmacogenetica integrata: come cambierà la psichiatria?
Verso un modello integrato di cura
Il futuro della psichiatria personalizzata risiede nell’integrazione armonica tra farmacogenetica, biomarcatori e monitoraggio clinico continuo.
Questo modello di cura integrato permette di combinare le informazioni genetiche (test farmacogenetici), le misure biologiche (biomarcatori) e la valutazione clinica sistematica della risposta terapeutica, offrendo una strategia globale per ottimizzare la gestione dei disturbi psichiatrici.
In concreto, il modello integrato prevede che la prescrizione farmacologica non si basi esclusivamente sulla diagnosi e sulla sintomatologia riferita dal paziente, ma anche su informazioni precise e oggettive relative al suo profilo genetico e biologico.
La terapia, così progettata, viene successivamente perfezionata attraverso un monitoraggio regolare della risposta clinica, che consente ulteriori adattamenti mirati nel tempo.
Potenzialità e vantaggi del modello integrato
L’approccio integrato presenta numerosi vantaggi clinici, terapeutici e anche economici, tra i quali si segnalano:
- Maggiore precisione terapeutica:
La combinazione delle informazioni genetiche e biologiche consente di identificare precocemente il farmaco più appropriato per ciascun paziente, evitando inefficacia terapeutica e riducendo la probabilità di effetti avversi. - Riduzione dei tempi terapeutici:
La possibilità di predire con maggiore affidabilità la risposta farmacologica permette di abbreviare significativamente il periodo di “tentativo ed errore” che attualmente caratterizza la terapia psichiatrica, migliorando così la qualità di vita dei pazienti e accelerando il raggiungimento della remissione. - Gestione più efficace dei casi complessi:
Pazienti resistenti o con scarsa tolleranza ai trattamenti convenzionali beneficiano particolarmente dell’approccio integrato, in grado di personalizzare con precisione la scelta terapeutica e il dosaggio sulla base di parametri oggettivi. - Aumento della sicurezza dei trattamenti:
Un modello basato sulla farmacogenetica integrata consente di ridurre drasticamente il rischio di effetti collaterali gravi, favorendo la prescrizione di trattamenti sicuri e tollerabili sin dalle prime fasi della terapia. - Efficienza economica:
A lungo termine, la riduzione di tentativi terapeutici infruttuosi e delle complicanze associate rappresenta un significativo risparmio economico per i sistemi sanitari, grazie alla migliore allocazione delle risorse disponibili.
Conclusioni
Nonostante le grandi potenzialità della farmacogenetica integrata, la sua implementazione efficace nella pratica clinica quotidiana richiede di affrontare alcune sfide rilevanti: innanzitutto è necessario realizzare studi prospettici rigorosi, randomizzati e multicentrici che ne dimostrino chiaramente i vantaggi clinici ed economici rispetto agli approcci convenzionali; inoltre, occorre standardizzare i test genetici e i biomarcatori intermedi, rendendoli interoperabili e facilmente accessibili per garantire risultati affidabili e comparabili nei diversi contesti clinici.
Parallelamente, risulta fondamentale investire nella formazione specifica dei clinici per assicurare che essi siano in grado di interpretare correttamente e utilizzare al meglio le informazioni derivanti da tali test.
Altri aspetti critici riguardano le questioni etiche e di privacy legate alla gestione responsabile dei dati genetici e clinici dei pazienti, che richiedono normative chiare e solide garanzie di protezione, nonché i costi e l’accessibilità economica di queste tecnologie, ancora proibitivi in molti contesti socioeconomici svantaggiati.
Affrontare con successo tali sfide richiederà un impegno coordinato tra ricercatori, clinici, istituzioni sanitarie e politiche, ma l’enorme potenziale della farmacogenetica integrata rende questo sforzo non solo auspicabile, ma necessario per rivoluzionare concretamente il futuro della pratica psichiatrica.